A tabela periódica
É necessário gravar a tabela periódica para fazer a prova do ENEM/UERJ/CN/EAM/EXPCEX? Como é a tabela periódica atualmente? O que já entrou em desuso pela IUPAC? Quais são as informações que há na tabela periódica?
Compreender a tabela periódica é essencial para estudar química. Dependendo da posição que o elemento químico nela ocupa, podemos prever suas propriedades químicas. Por isso, se o concurso em que você almeja passar tem química, é fundamental que você saiba ler a tabela periódica.
A tabela organiza os elementos químicos em ordem crescente de número atômico. Ela atualmente possui um total de 118 elementos químicos, cada um com seu símbolo, número atômico e número de massa. Algumas tabelas também trazem dados adicionais, como a distribuição eletrônica em camadas de cada elemento.
São muitos os dados que constam na tabela periódica. Mas fique calmo! Não é necessário gravar a tabela periódica para realizar provas de concursos militares e vestibulares. Com exceção da prova do ENEM, a tabela periódica em preto e branco estará disponível para consulta no final do caderno de questões. Desta forma, se você precisar dela durante a prova, procure por ela nas últimas páginas do exame. Embora o ENEM não disponibilize a tabela periódica para consulta, a questão trará todos os dados de que você necessita para resolver a questão. Agora, vamos aprender a ler a tabela periódica!

Os elementos químicos são representados em pequenos retângulos dispostos lado a lado, onde é possível ler as informações listadas acima. O número atômico corresponde ao número de prótons que o átomo possui em seu núcleo. Átomos de mesmo número atômico pertencerão ao mesmo elemento químico. Esta é a principal propriedade que caracteriza um dado átomo.
O símbolo do átomo corresponde a uma letra maiúscula (Ex.: H) ou a uma letra maiúscula seguida de uma letra minúscula (Ex.: He). Abaixo do símbolo, podemos ler a massa atômica do elemento químico. Esta massa corresponde à massa média ponderada de todos os isótopos pertencentes àquele elemento.
Dependendo da tabela periódica, podemos consultar outros dados, como o estado físico e se o elemento químico é natural ou sintético. Abaixo, temos a tabela periódica atualizada disponibilizada pela Sociedade Brasileira de Química.

Tabela periódica. Fonte: SBQ. Disponível em: https://www.sbq.org.br/anexos/tabela%20periodica_SBQ_3.0_set2023.pdf
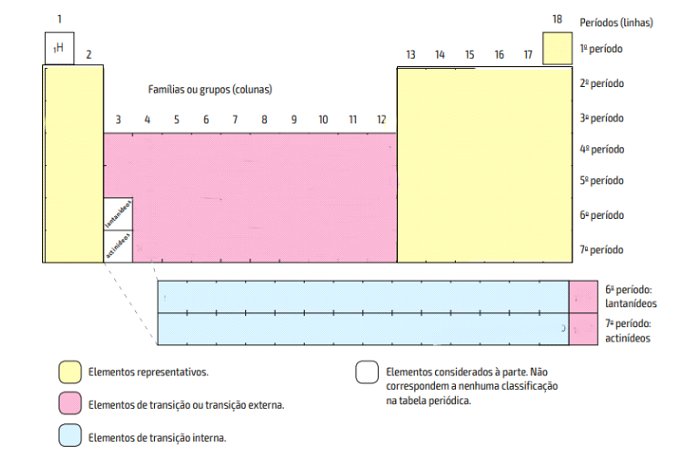
A tabela periódica é composta por 7 linhas, que correspondem aos períodos, e por 18 colunas, que correspondem aos grupos ou famílias. Elementos químicos que se encontram no mesmo período possuem o mesmo número de camadas eletrônicas preenchidas por elétrons. Elementos químicos que se encontram no mesmo grupo possuem propriedades semelhantes.
Os elementos representados em amarelo e em verde são chamados de lantanídeos e actinídeos, respectivamente. Os lantanídeos se encontram no sexto período da tabela periódica, enquanto os actinídeos se encontram no sétimo período da tabela. Representá-los na parte de baixo da tabela permite que esta possa ser representada de forma compacta e legível. Caso contrário, a tabela periódica seria representada em sua forma expandida, da maneira como se encontra na figura abaixo:

Elementos representativos e de transição:
Os grupos 1, 2, 13, 14, 15, 16, 17 e 18 são denominados elementos representativos.
Os grupos 3 a 12 são chamados de elementos de transição externa.
Os lantanídeos e actinídeos são chamados de elementos de transição interna.
As famílias das tabelas periódicas:
Alguns grupos ou famílias da tabela periódica recebem nomes especiais. Quando a família não possui um nome especial, dá-se àquele grupo o nome do primeiro elemento químico pertencente à família. É fundamental que o candidato ao vestibular e aos concursos militares saiba identificar cada uma das famílias dos elementos representativos.

Famílias da tabela periódica. Fonte da imagem: todamatéria. Disponível em: https://www.todamateria.com.br/familias-da-tabela-periodica/
Na imagem acima, pode-se observar que os grupos estão numerados de 1 a 18 e também estão numerados utilizando-se uma representação de letra seguida de número (Ex.: 1A, 2A, etc). Esta numeração - de letra seguida de número - já foi muito utilizada, mas atualmente não é mais recomendada pela IUPAC.
As famílias dos elementos representativos são:

O hidrogênio, apesar de ser posicionado acima do lítio na tabela periódica, não é considerado um metal alcalino. Este elemento possui propriedades únicas que fazem com que ele não se enquadre em nenhum grupo da tabela.
Classificação dos elementos químicos:
Os elementos químicos podem ser classificado como metais, ametais, gases nobres e hidrogênio.
A classificação semimetais ou metalóides está em desuso. Os semimetais eram um grupo de elementos químicos que se posicionavam entre os metais e os ametais e que, teoricamente, teriam propriedades intermediárias às duas classes. Tais elementos seriam: boro, silício, germânio, arsênio, antimônio e telúrio. É importante ressaltar que, apesar desta classificação se apresentar em diversas tabelas periódicas, a IUPAC não a reconhece. Além disso, desde 2001, a Sociedade Brasileira de Química não cita tal classificação em suas tabelas. Segundo a SBQ, o germânio, atimônio e polônio são metais, enquanto boro, silício, arsênio e telúrio são ametais.
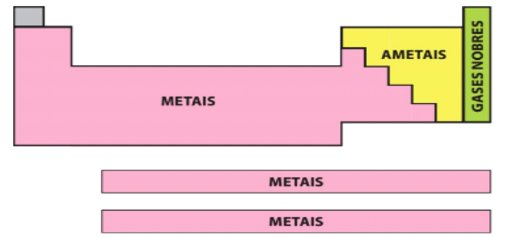
Classificação dos elementos químicos. Fonte: desconhecida.
Metais: Constituem a maior parte dos elementos químicos. São bons condutores de calor e eletricidade. São sólidos em temperatura ambiente (com exceção do mercúrio), maleáveis, podendo serem transformados em lâminas muito finas, e dúcteis, podendo serem transformados em fios. Possuem também brilho característico (brilho metálico), cor acinzentada ou prateada (exceto ouro e cobre), e tendência a perder elétrons, formando cátions.
Ametais: Geralmente são maus condutores de calor e eletricidade. Podem ser encontrados nos estados sólido, líquido ou gasoso em temperatura ambiente. Não são dúcteis e nem maleáveis, não possuem brilho e são tendentes a ganhar elétrons, formando ânions.
O grafite, uma das formas alotrópicas do carbono, é uma das exceções à regra, pois conduz eletricidade. O iodo também possui uma exceção: ele é um sólido de cor acinzentada que possui brilho.
Gases nobres: São gases inertes , ou seja, não possuem tendência a reagir com outros átomos. São encontrados na natureza na forma de átomos isolados.
Hidrogênio: possui tendência a reagir com metais e ametais, possuindo comportamento químico diferenciado em cada uma das duas situações. Quando na forma molecular, forma o gás H2, um gás menos denso que o ar e inflamável.
Arquivos
Qual é a sua reação?